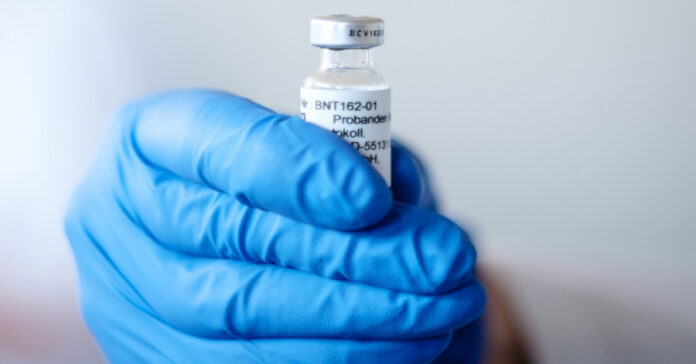
Αίτηση στον Ευρωπαϊκό Οργανισμό Φραμάκων (ΕΜΑ) για την υπό όρους έγκριση του εμβολίου τους κατά του κορονοϊού κατέθεσαν οι εταιρείες Pfizer και BioNTech, με τον ΕΜΑ να κάνει σήμερα γνωστό πως, αν τα δεδομένα είναι επαρκή, θα ολοκληρώσει την αξιολόγηση του υποψήφιου εμβολίου μέχρι τις 29 Δεκεμβρίου.
Θυμίζουμε πως Pfizer και BioNTech ανακοίνωσαν στις 18 Νοεμβρίου τα τελικά αποτελέσματα της τρίτης φάσης δοκιμών του εμβολίου τους κατά της covid-19, σύμφωνα με τα οποία αυτό είναι κατά 95% αποτελεσματικό στην πρόληψη της μόλυνσης, χωρίς να έχει προκαλέσει σοβαρές παρενέργειες. Στις 20 Νοεμβρίου οι δύο εταιρείες είχαν υποβάλει αίτηση και στις αρμόδιες αρχές των ΗΠΑ.
Ο EMA ανακοίνωσε επίσης πως έχει λάβει αίτηση για άδεια διάθεσης στην αγορά και του υποψήφιου εμβολίου της Moderna Inc κατά της Covid-19 και πως, αν τα δεδομένα είναι επαρκή, θα ολοκληρώσει την αξιολόγησή του για το εμβόλιο αυτό μέχρι τις 12 Ιανουαρίου.
Την τελική έγκριση για την κυκλοφορία των εμβολίων κατά της νόσου Covid-19 αναμένεται να δώσει η Ευρωπαϊκή Επιτροπή, λίγες ημέρες αφού ο δώσει την έγκρισή του ο ΕΜΑ. Σύμφωνα με τους κανόνες της ΕΕ, ο EMA εισηγείται την αδειοδότηση ενός φαρμάκου ή εμβολίου και η Ευρωπαϊκή Επιτροπή εκδίδει άδεια κυκλοφορίας με βάση των γνωμοδότηση της ρυθμιστικής αρχής.
Με πληροφορίες από το ΑΠΕ-ΜΠΕ
ΣΧΕΤΙΚΑ ΑΡΘΡΑ
- Εμβόλια Covid-19: Το στοίχημα για την αλυσίδα μεταφοράς-αποθήκευσης-διανομής
- Εμβόλια για Covid-19: Τι σημαίνει η αποτελεσματικότητα 95% στις δοκιμές
- ΗΠΑ: Pfizer και BioNTech καταθέτουν σήμερα αίτημα αδειοδότησης για το…
- Επισφραγίστηκε η συμφωνία Ευρωπαϊκής Επιτροπής και Pfizer/BioNTech
- Covid-19: Αποτελεσματικότητα κατά 90% για το εμβόλιο των Pfizer και…